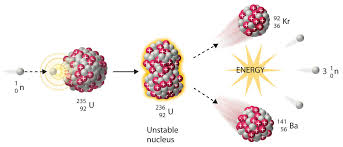
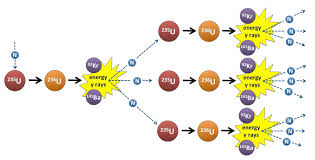
همیشه بعد یک شکافت هسته ای 3 نوترون خارج نمی شود بلکه ممکن است با توجه به شرایط واکنش، یک تلور و 2 نوترون خارج شود.
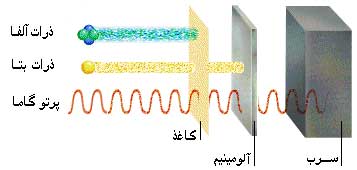
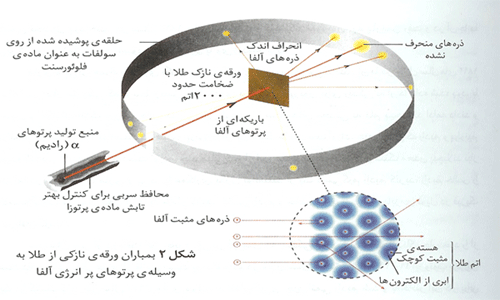
در جلسات قبل 3 نوع پرتوی رادیو اکتیویته ذکر شده بود(آلفا، بتا و گاما) که دوتای اولی می توانستند پس از تشعشع، نوع هسته ای که در آن بودند را تغییر دهند. در این جلسه، بیشتر وارد این موضوع می شویم.
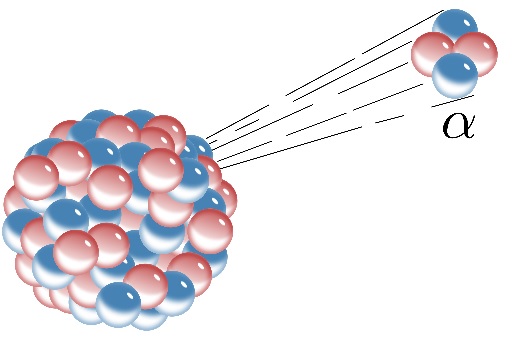
تشعشع آلفا:
با تشعشع پرتوی آلفا، 2 پروتون و 2 نوترون از هسته خارج می شود یعنی 2 تا از عدد اتمی و 4 تا از عدد جرمی کم می شود.
برای مثال اگر یک هسته ی اورانیوم 238 آلفا بتاباند، آن موقع 4 عدد جرمی از دست می دهد و 2 عدد اتمی و تبدیل می شود به توریوم 234 و با 2 بار تابش دیگر، رادیم 226 خواهیم داشت.
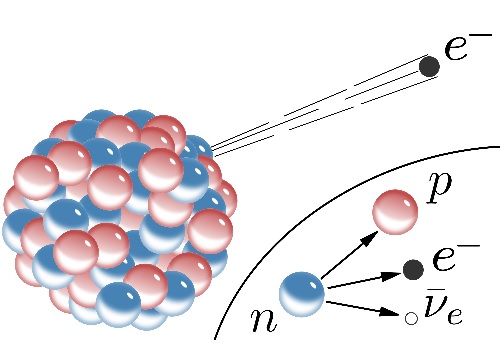
تشعشع بتا:
وقتی تشعشع بتا اتفاق می افتد، عدد جرمی و بار ماده تغییر نمی کنند و یکی به عدد اتمی اضافه می شود چون بتا پس از واپاشی نوترون به دست می آید به این شکل که پس از واپاشی، یک پروتون تولید می شود و از آن جایی که جرم نوترون بیشتر از پروتون است، مقدار جرم باقیمانده به شکل ذراتی شبیه به الکترون از هسته خارج می شود.
در این جا هیچ ربطی به الکترون وجود ندارد ، پروتون یکی زیاد می شود و عدد جرمد تغییری نمی کند چون یکی به پروتون ها اضافه شده و یکی از نوترون ها کم شده و عدد جرمی مجموع این دوتاست.
تمام عناصر سنگین دچار واپاشی می شوند و این واپاشی ها آن قدر ادامه پیدا می کنند تا به عنصر سرب(pb)برسند و سپس پایدار می شوند.
جوش هسته ای برعکس شکاف هسته ای است و در آن چند عنصر را در گرما و فشار زیاد به هم می چسبانیم. این عنصر واپاشی می شود و بعد عناصری سبک تر و انرژی ای به مراتب بیشتر از شکافت ایجاد خواهد شد.
واکنش های هسته ای:الف)واپاشی هسته ای ب) شکافت هسته ای ج)جوش هسته ای
واپاشی خود به خود و 2 مورد دیگر با انرژی ای از بیرون اتم اتفاق می افتند مثلا در خورشید 4 هلیم در اثر فشار و گرمای زیاد 1 هیدروژن و مقدار فراوانی انرژی می سازند و 1 دوتریم با یک تریتیم در جوش هسته ای انرژی فراوان به همراه 1 هلیم و 1 نوترون می سازند.

 ==> - ==> e
==> - ==> e ==>موج ==> خنثی
==>موج ==> خنثی